- 2026年4月18日
カルシニューリン阻害薬の腎組織内分布と滞留性の比較検証:基礎研究
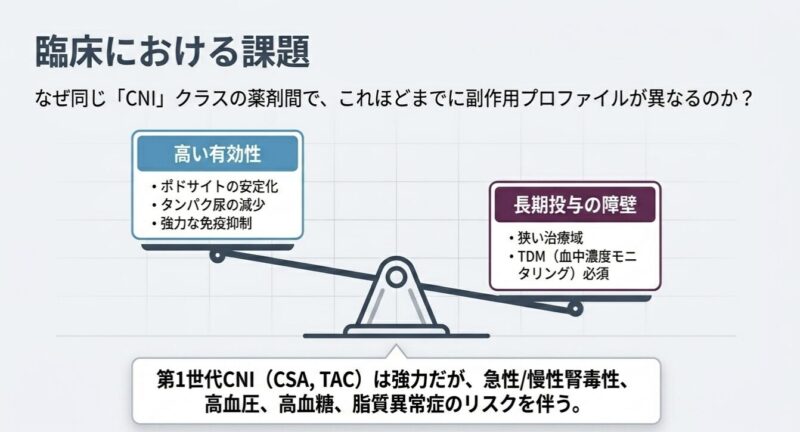
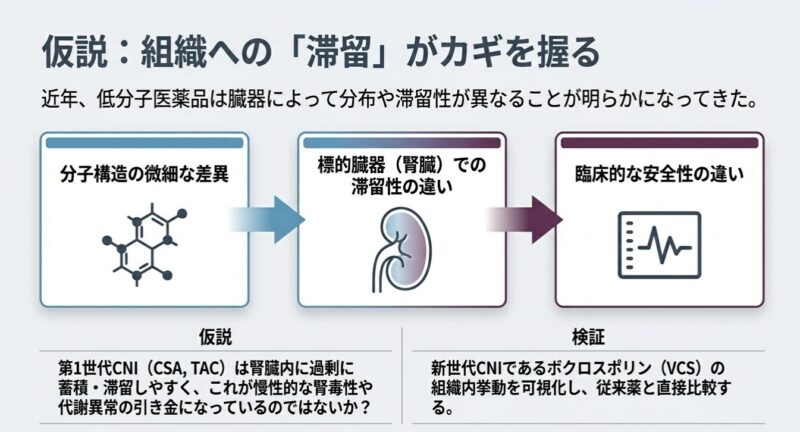
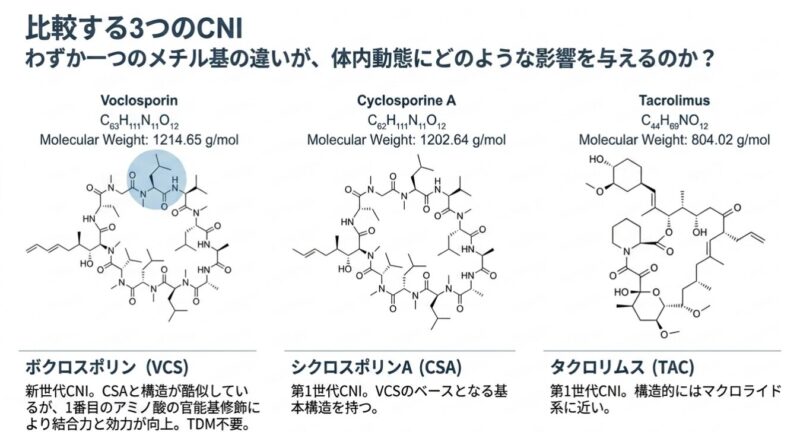
カルシニューリン阻害薬(CNI)は、T細胞のインターロイキン-2(IL-2)産生を抑制する免疫抑制作用に加え、糸球体ポドサイトのシナプトポジン脱リン酸化阻害を介した細胞骨格安定化作用を有し、ループス腎炎(LN)治療の基石となっています。しかし、第一世代CNIであるシクロスポリンA(CSA)やタクロリムス(TAC)は、慢性的な腎毒性や代謝異常(高血糖、脂質異常症)が長期投与の障壁となってきました。第二世代CNIであるボクロスポリン(VCS)と第一世代薬の腎組織内動態をMALDI-MSI(マトリックス支援レーザー脱離イオン化質量分析イメージング)を用いて比較した研究成果をまとめました。
【研究の目的と手法】
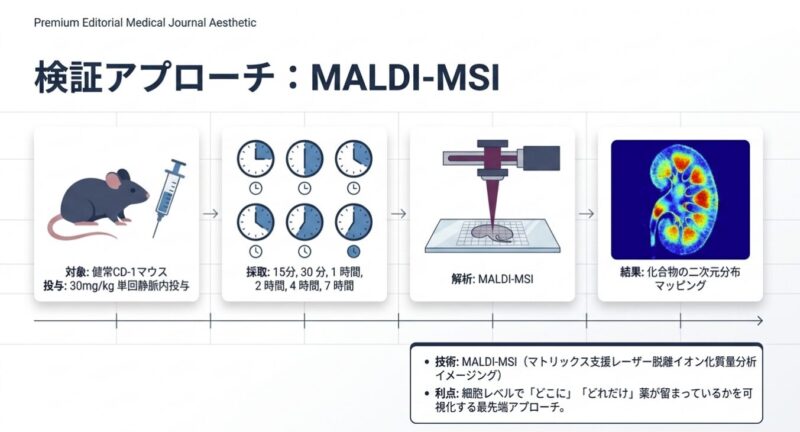
健康なCD-1マウスを用い、VCS、CSA、TAC(各30 mg/kg)を単回静脈内投与した後の腎組織内における薬剤の分布と滞留時間をMALDI-MSIにより経時的(15分〜7時間)に評価。MALDI-MSIは組織切片上の化合物のイオン強度を二次元画像化する手法であり、従来の組織均質化法では困難であった「組織内のどの部位にどの程度薬剤が留まっているか」の可視化を可能にします。
【主要な研究結果】
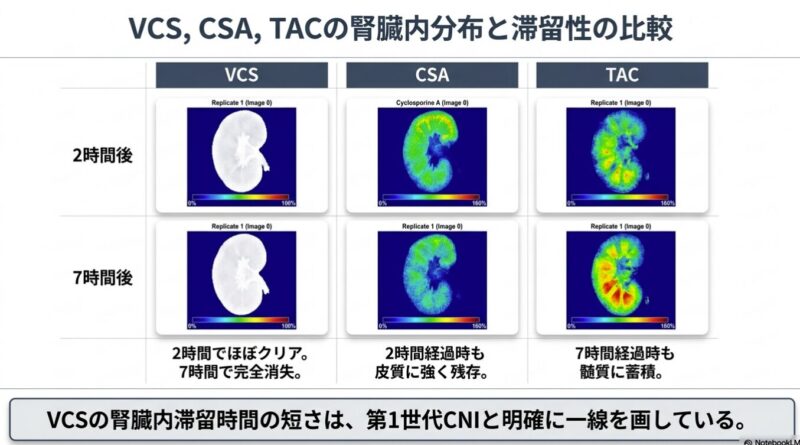
1. 腎組織内分布と滞留性の顕著な差異
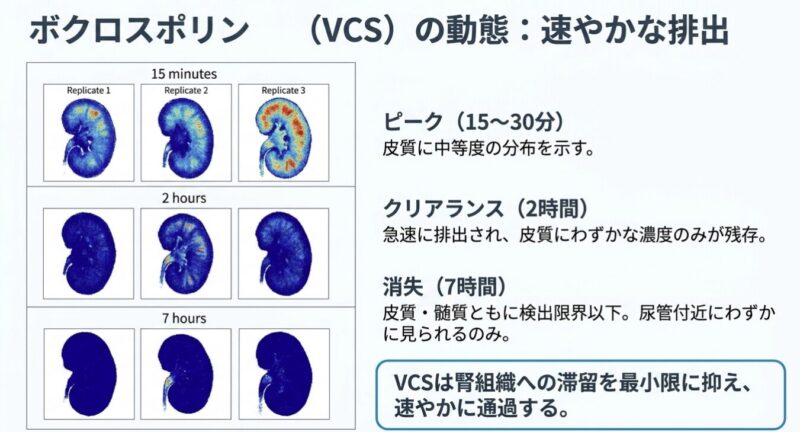
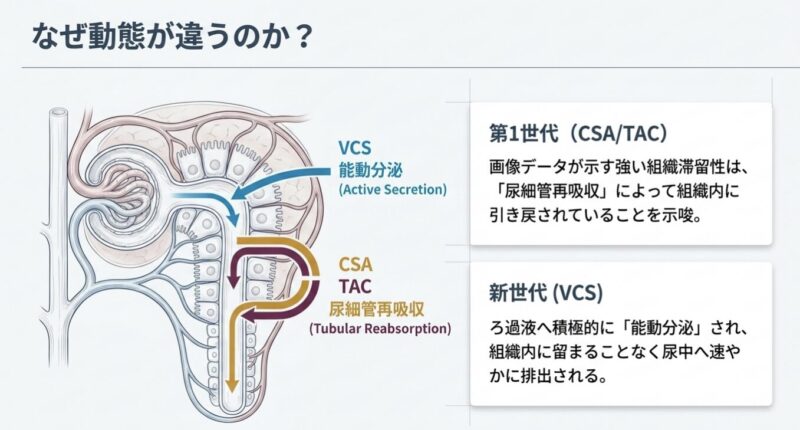
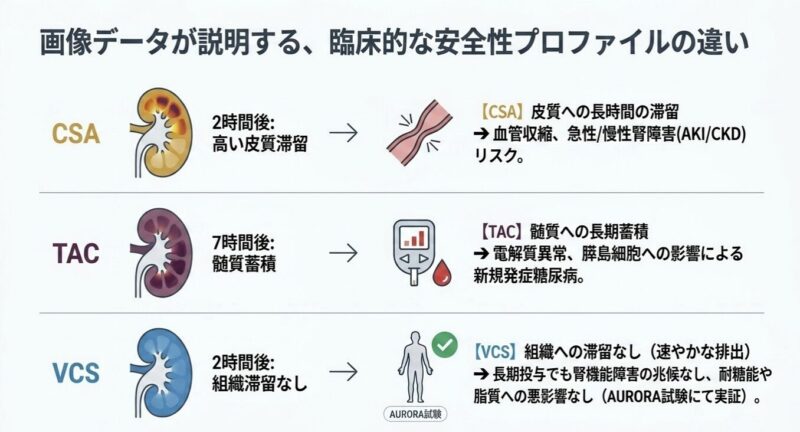
- ボクロスポリン(VCS): 投与15〜30分後に皮質を中心とした中等度の分布がピークに達し、その後速やかに消失しました。投与2時間後には皮質に低濃度が残るのみとなり、7時間後にはほぼ完全に消失しました。
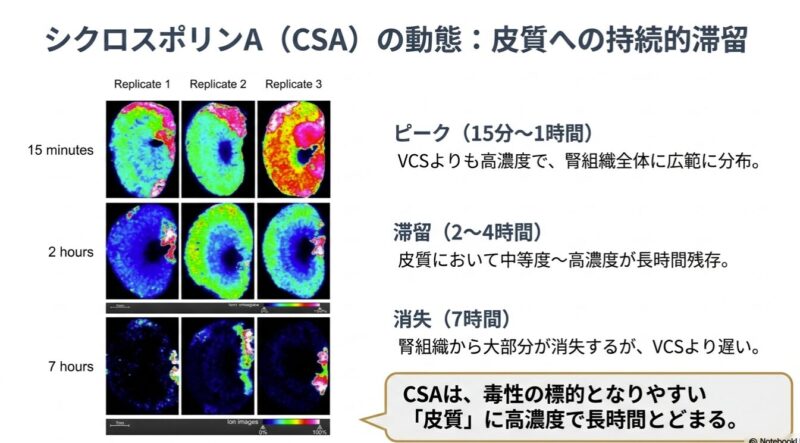
- シクロスポリンA(CSA): VCSよりも高濃度で腎組織全体にびまん性に分布し、皮質における滞留性も高く、投与4時間後でも中等度の濃度が維持されていました。
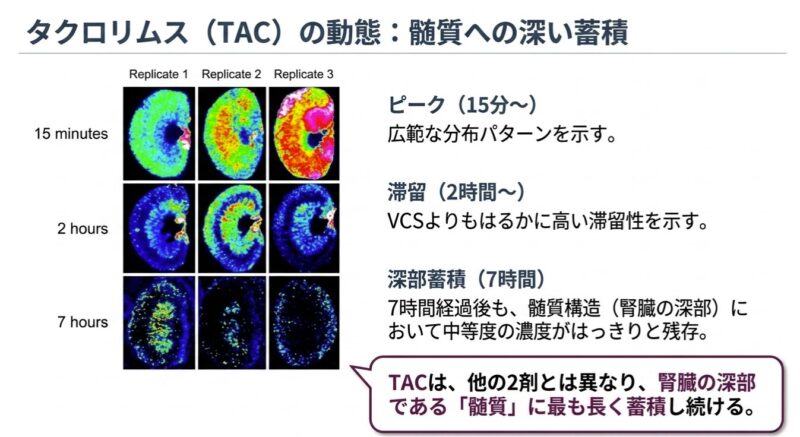
- タクロリムス(TAC): 腎組織全体にびまん性に分布し、特に髄質において顕著な滞留性を示し、投与7時間後でも中等度の濃度が検出されました。
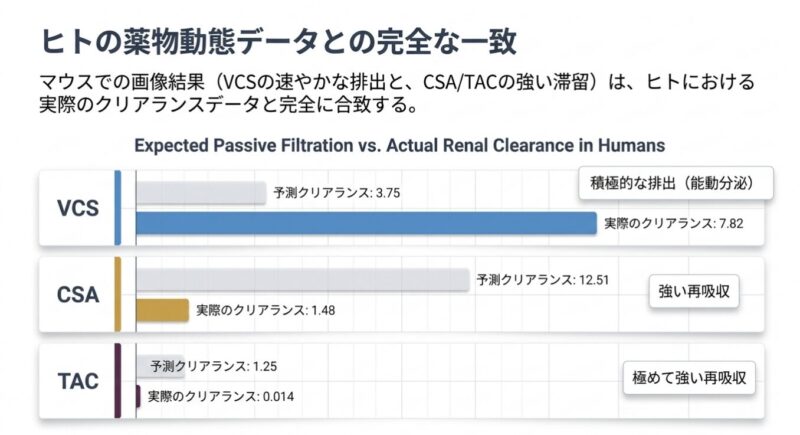
2. ヒトにおける腎クリアランスとの相関
今回のマウスでの観察結果は、ヒトにおける腎排泄機序と整合しています。ヒトにおいてCsAとTacの腎クリアランスは受動濾過期待値のそれぞれ約10%および2%未満であり、尿細管での「再吸収」が示唆されます。一方、VCSの腎クリアランスは受動濾過期待値の約200%であり、近位尿細管における「能動分泌」が優位(支配的)であることが示されています。
【医学的考察と臨床的意義】
VCSが他のCNIと比較して腎組織内での滞留時間が極めて短いことが示されています。CsAやTacが腎組織(特に尿細管上皮細胞)に長時間留まることは、直接的な細胞毒性や血行動態の変化を介した急性・慢性腎障害の一因と考えられています。VCSの「迅速な消失」と「能動分泌」という特性は、腎臓への累積的な曝露を最小限に抑え、臨床試験(AURORA試験)で示された良好な腎安全性プロファイルを裏付ける薬理学的根拠となりえます。
また、VCSは第一世代薬と異なり、治療薬物モニタリング(TDM)を必要としない安定した薬物動態を示し、脂質代謝や血糖管理においても有利なエビデンスを有しています。これらの特性は、LN患者における3年以上の長期寛解維持療法において、腎機能を保護しつつステロイドを減量(ステロイド・ミニマム戦略)するための強力な武器とも言えます。



Pharmaceutical Research. 2026. Published online: 08 January 2026. doi:10.1007/s11095-025-03943-y.
柏五味歯科内科リウマチクリニック
ホームページ