- 2026年4月18日
ループス腎炎治療におけるボクロスポリンの有効性と安全性:AURORA 1試験(第3相臨床試験)の解析
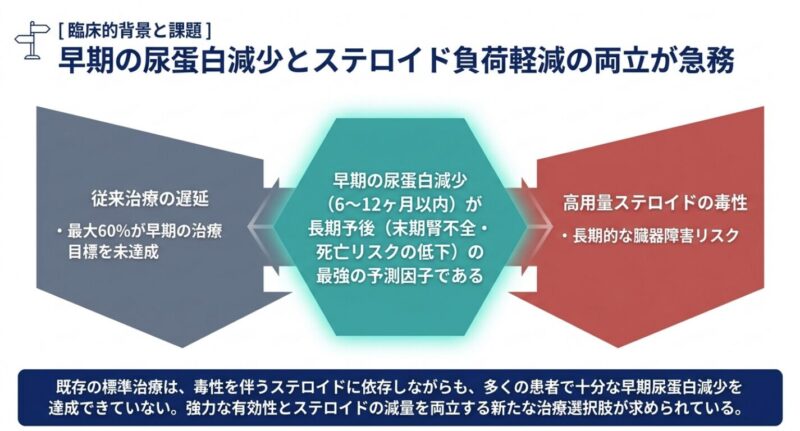
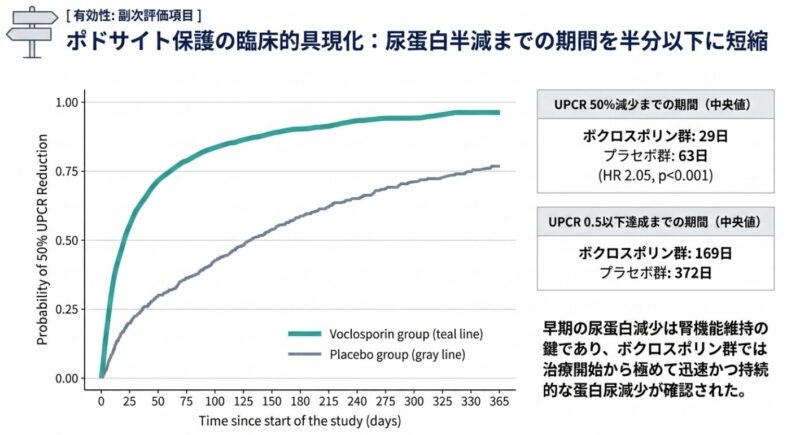
活動性ループス腎炎(LN)は、全身性エリテマトーデス(SLE)患者の約20%が診断後10年以内に末期腎不全(ESKD)へ進行する重篤な合併症です。治療の主眼は腎機能の保持と死亡率の低下にあり、特に治療開始後6〜12ヶ月以内の早期の蛋白尿減少が長期予後の最良の予測因子であることが示されています。新規カルシニューリン阻害薬(CNI)であるボクロスポリンの有効性を検証した国際共同第3相試験「AURORA 1」の結果に基づき、その臨床的意義を考察します。
【PICO:臨床試験の構成】
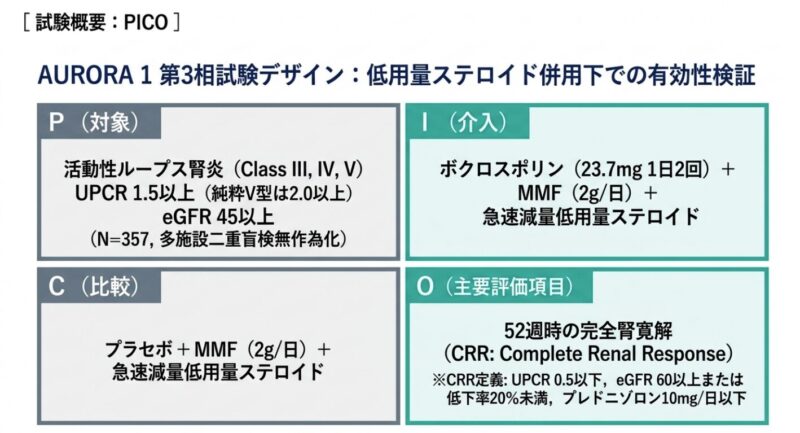
- P(Population): アメリカリウマチ学会(ACR)基準を満たすSLE患者のうち、生検でClass III、IV、V(単独または混合)の活動性LNを確認。ベースラインのUPCR≧1.5 mg/mg(純粋なClass Vは≧2 mg/mg)、eGFR>45 mL/min/1.73 m²の患者計357名。
- I(Intervention): ボクロスポリン(23.7 mg 1日2回)+ ミコフェノール酸モフェチル(MMF 2g/日)+ ステロイド急速減量(16週目までに2.5 mg/日まで減量)。
- C(Comparison): プラセボ + MMF(2g/日)+ ステロイド急速減量。
- O(Outcome): 52週時点の完全腎反応(CRR)達成率。CRRの定義は、①UPCR≦0.5 mg/mg、②eGFRの安定(≧60 mL/min/1.73 m²またはベースライン比20%以内の低下)、③レスキュー薬不使用、④低用量ステロイドの維持(週44〜52でプレドニゾン換算10mg以下)。
【主要な試験結果】
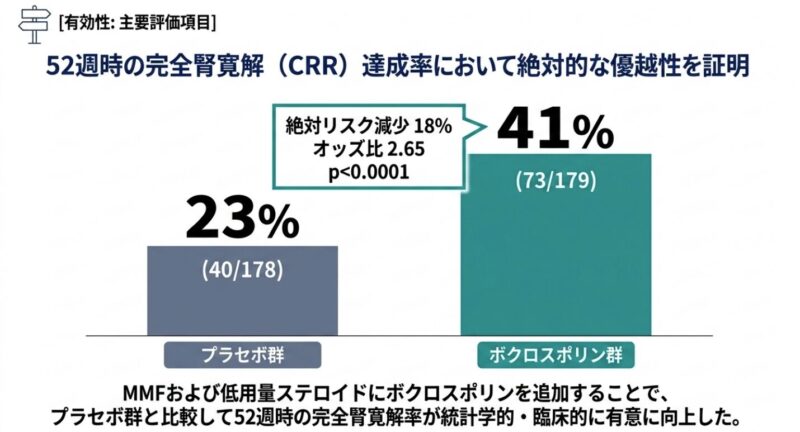
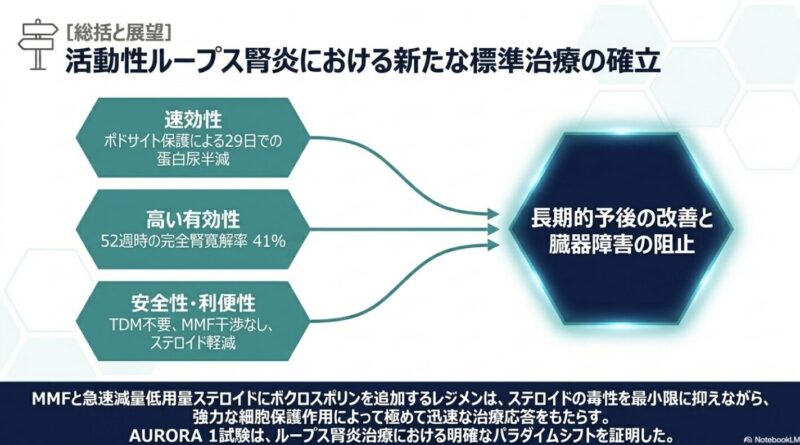
主要評価項目である52週時点のCRR達成率は、ボクロスポリン群で41%(73/179名)、プラセボ群で23%(40/178名)29日、プラセボ群で63日(ハザード比 2.05, p<0.001)であり、ボクロスポリンの迅速な抗蛋白尿作用が確認された。
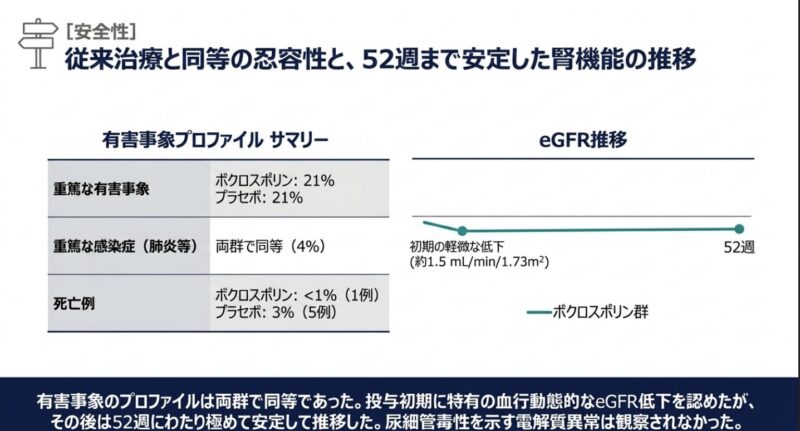
安全性については、重篤な有害事象(SAE)の発生率は両群とも21%で同等であった。感染症関連のSAE(主に肺炎)も両群で4%と均衡しており、ボクロスポリンの追加による過度な免疫抑制リスクの増大は認められなかった。また、ボクロスポリン群の死亡は1名(<1%)に対し、プラセボ群は5名(3%)であった。
【医学的考察と臨床的意義】
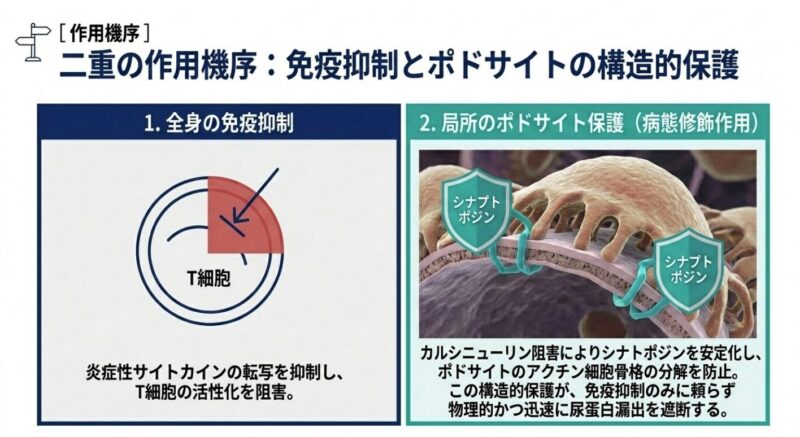
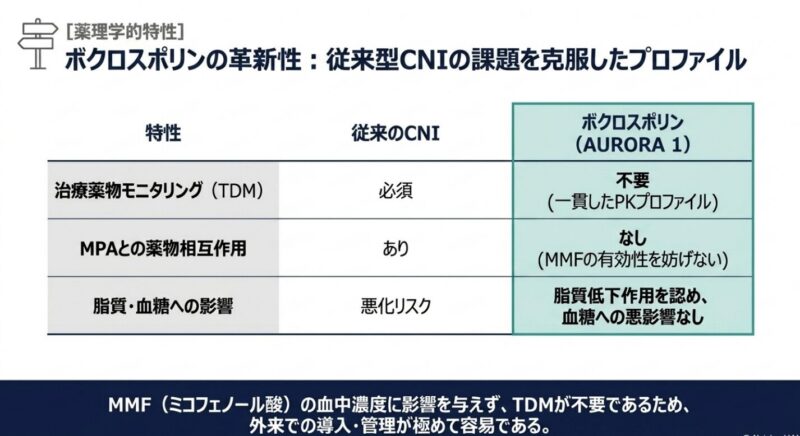
ボクロスポリンは、従来のCNIと比較して安定した薬物動態を有し、治療薬物モニタリング(TDM)を必要としない利点がある。作用機序としては、T細胞活性化の抑制(IL-2転写阻害)に加え、ポドサイト(足細胞)内のシナプトポジンを安定化させ、アクチン骨格の崩壊を防ぐ直接的な足細胞保護作用を併せ持つことが示唆されている。 本試験の意義は、「ステロイド曝露量を最小化しつつ、早期の腎反応達成率を向上させる」三剤併用療法の有用性を大規模な多施設共同試験で証明した点にある。特に、多様な人種を含む集団で一貫した効果が示されており、現代のLN導入療法における標準的な選択肢としての地位を確立したと言える。

Lancet 2021; 397: 2070–80. doi: 10.1016/S0140-6736(21)00578-X
柏五味歯科内科リウマチクリニック
ホームページ